原标题:西湖大学黄晶:基于深度学习的蛋白质力场模型优化,启示未来药物设计新思路
科学智能(AI for Science)通过学习、模拟、预测和优化自然界与人类社会的各种现象和规律,从而推动科学发现和创新。络绎科学发起「科学智能 50 人」访谈计划,旨在邀请科学智能领域优秀的专家代表,希望通过系列访谈,为广大读者呈现一个更全面、深入的科学智能领域的发展现状和前沿洞察。
AI 技术亦是如此。在近 70 多年间,AI 技术得到快速发展并与科学研究深度交叉融合,催生了一种新兴科技形态——AI for Science(科学智能,也称 AI4S)。这是近年兴起的一种将人工智能和科学相结合的趋势,即通过利用机器学习或者其他 AI 技术提出和解决科学研究中的问题。
当前,AI for Science 已经发展为全球人工智能发展的新前沿,这种模式正在加速科学研究的范式变革,有望为科学研究领域带来模式重构和新一轮科技革命。此前,达摩院在《达摩院 2022 十大科技趋势》中也提到,人工智能正在成为科学家的新生产工具,AI for Science 催生了科研新范式。
为了进一步了解 AI for Science 的发展现状,近日生辉采访了西湖大学生命科学学院计算生物物理与药物设计实验室负责人黄晶博士,他介绍了自己在 AI+ 生物制药领域的研究工作以及对 AI for Science 的见解。

黄晶本科毕业于清华大学物理系,在瑞士巴塞尔大学化学系获得博士学位,长期从事基于分子动力学模拟的模型与算法开发。2017 年加入西湖大学并成立独立实验室,实验室的重点研究方向是开发生物大分子的计算模型和模拟算法,提升生物分子动力学模拟和计算机辅助药物设计的精度和效率。
黄晶实验室的主要研究可以分为三大方向,一是提升分子力场(Force fields)精度和效率,尤其是蛋白质力场;二是研究蛋白质动力学和功能之间的关系,解析物质如何跨膜转运;三是通过算法设计小分子药物,主要集中在抗感染和抗肿瘤领域。
“这三个研究方向之间相互支持,相互促进,且都取得了一些积极的结果。在分子力场和计算模型方面的研究支持了蛋白动力学研究,尤其可以更好描述小分子和蛋白质之间的相互作用,而这有助于小分子药物设计和研发。”黄晶说。
其中,分子力场是分子模拟的基础,也是分子结构的一种简化模型,其可以计算和描述原子之间的相互作用。分子力场的精度决定了计算模拟方法所得结果的质量,开发更准确的分子力场对于生物分子建模、分子动力学模拟、基于结构的药物设计等领域均具有决定性的意义。
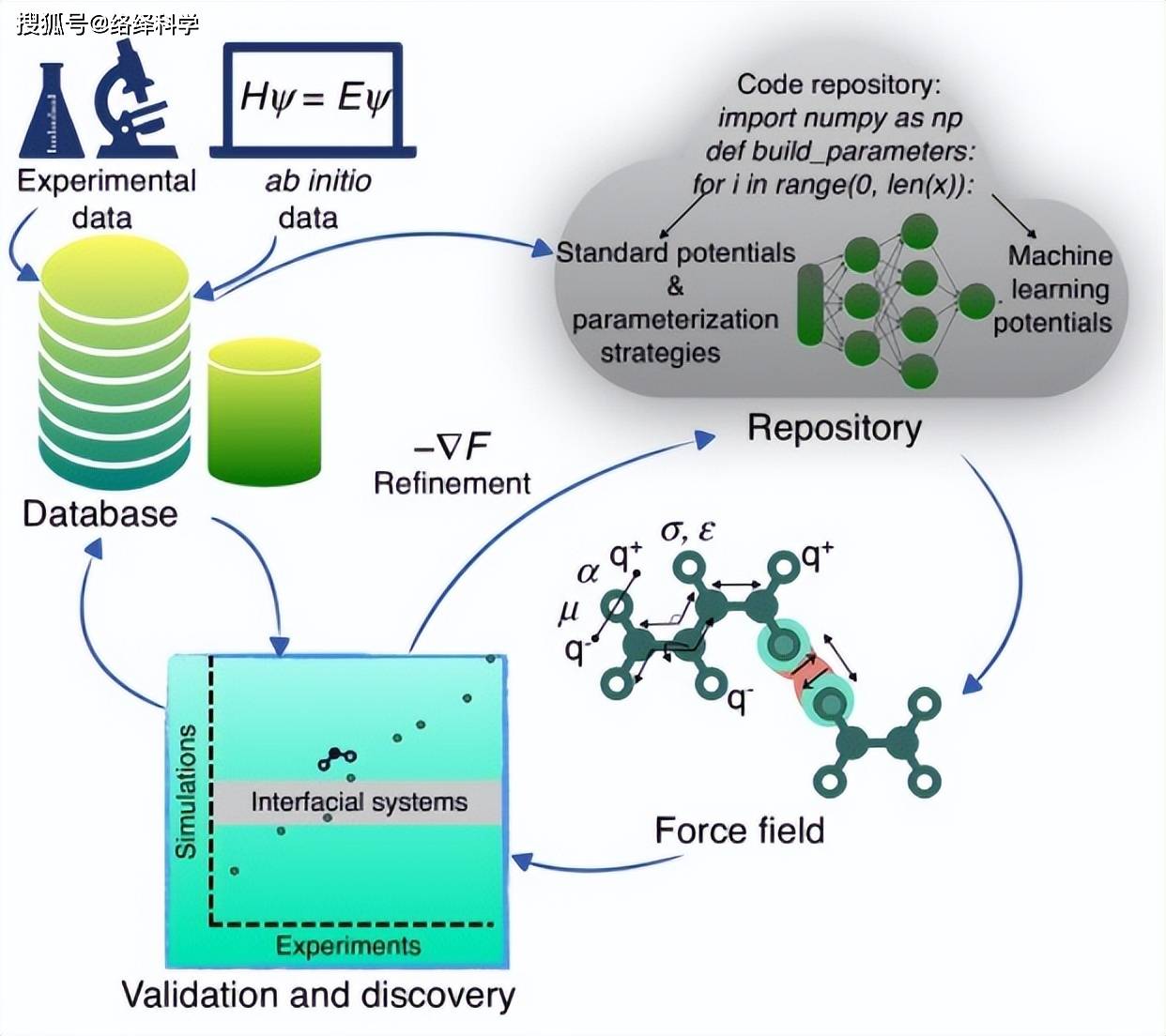
(来源:Current Opinion in Chemical Engineering)
黄晶解释道,分子力场是计算生物学的基础模型,这是一种底层技术支持,它在计算生物学领域的各个方面都在发挥着重要作用。
据悉,黄晶团队正在通过技术创新构建更准确的力场模型,从而对蛋白质、小分子和蛋白质的相互作用更准确建模。现阶段,该团队已经开发出一系列针对生物大分子的模型和算法。
据黄晶介绍,在计算模型方面,团队的技术创新点主要得益于深度学习模型,将深度学习中的多种工具借用到力场优化中。比如说,直接优化实验观测值对于力场参数的导数,而自动微分技术使得此前难以实现的方法成为可能;将随机梯度下降等新的数学优化工具用于力场模型的构建和优化,提升调参效果;还采用多种深度学习工具解决了高维参数空间搜索等难题。
算法方面,该团队在 AI 辅助药物设计方面进行了一系列工作,尤其是基于结构的 AI 药物设计。比如说,近期黄晶研究团队提出了一种 SWIT 算法,这项工作实现了基于靶标三维结构的分子生成。研究的关键在于通过两个阶段分子对接构建靶标特异性训练集,基于消息传递网络模型(D-MPNN)构建打分函数预测模型,并将其以奖励函数的方式加入分子生成模型,以此指导生成模型产生与目标蛋白具有高亲和力的分子。
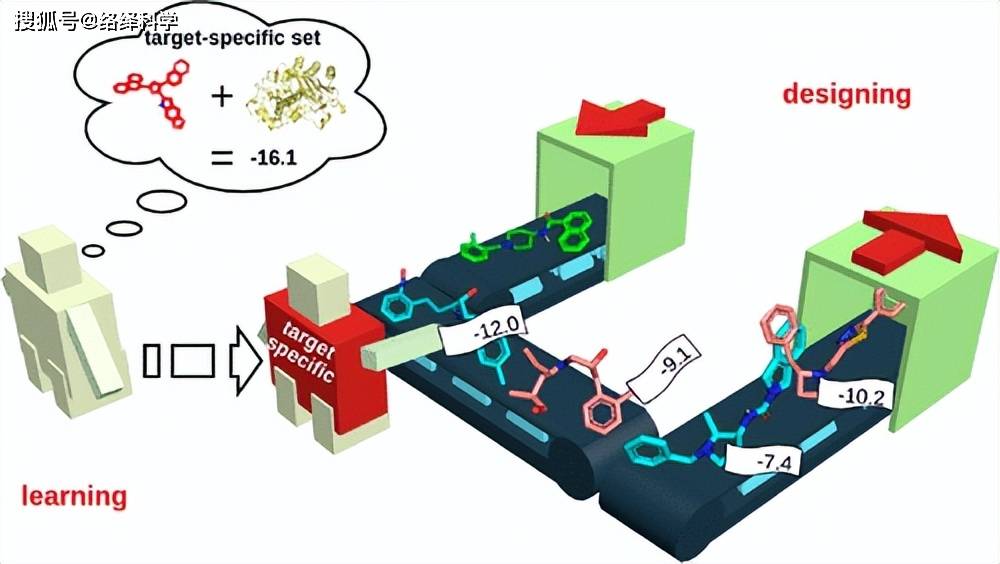
“通过这种方法,我们可以对完全没有已知分子活性信息的靶点生成大量能够与靶点口袋结合的分子,算法极其高效。我们基于这种方法可以理解给定靶点以及与靶点相结合的小分子的特性,并进行进一步的分析。”
基于这些计算模型和算法,过去两年内,该实验室通过 AI 算法设计出了多个小分子化合物且已经在黄晶联合创办的公司西湖制药推进转化工作。目前,抗感染的一个小分子化合物已经进入到临床 III 期试验,针对癌症的两个化合物现在正准备 IND 工作。
作为 AI 和科研深度融合的新兴科技形态,AI for Science 通常是指利用 AI 技术学习、模拟、预测和优化自然界和人类社会的各种现象和规律提出和解决各种科研问题,以推动科学发现和创新。这种新兴科技形态也被称之为“科学研究第五范式”。
“顾名思义,AI for Science 就是将 AI 应用到不同领域,并利用 AI 提出和解决科学问题。反过来,在 AI 研究和处理科学问题的过程中也会遇到技术难题,这些也会让科学家们思考 AI 技术的更多细节,这又会促进 AI 技术的进步和提升。我认为,AI 和科学是一场双向奔赴的征程,PP电子的官方网站两者相互促进,相互成就。”黄晶说。
黄晶进一步指出,随着深度学习等技术的持续发展,科学家们对 AI for Science 的理解也在不断深入,更深层次意识到 AI 确实是一种变革性的技术,对科学领域会带来更多革新。
“我相信,制药领域会是 AI 技术带来变革的一个重要应用场景之一。从靶点发现、苗头化合物、先导化合物再到临床前化合物,甚至是试验环节,AI 会在这个过程中发挥巨大的作用,包括提高缩短时间、增加成功率、节省成本等等。”
以靶点发现为例,AI 有潜力在这一环节发挥变革性的作用。黄晶指出,原创新药的源头在于对靶点生物学机制的理解,而随着 AlphaFold 以及一系列的 AI4S 研究工作,AI 逐步可以帮助科学家们进一步理解复杂生物学系统的工作机制,挖掘到新靶点,或者发现传统意义上旧靶点的新功能和新机制。从这一点来讲,这些传统靶点也会成为新靶点,AI 为这些靶点带来新的生物学认知。
“如果 AI 能完全实现这一点,不仅仅对整个生物制药领域带来巨大变化,甚至对整个人类健康事业也会是一个巨大的推进。”黄晶补充道。
声明:本文仅供科研分享,助力科学传播,不做盈利使用,如有侵权,请联系后台删除。返回搜狐,查看更多PP电子 app
Copyright © 2019-2023 PP电子「中国」平台网站 版权所有 备案号:鄂ICP备12015236号